2019年5月6日,代谢生物学领域国际知名学术期刊《Nature Metabolism》在线发表了上海科技大学生命科学与技术学院戚炜副教授(常任序列)课题组和武汉大学生命科学学院宋保亮教授课题组合作的研究论文《Gpnmb secreted from liver promotes lipogenesis in white adipose tissue and aggravates obesity and insulin resistance》。
该研究利用小鼠模型和人群样本,发现由肝脏分泌的Gpnmb蛋白可作用于脂肪组织,促进脂质合成,参与肥胖及胰岛素抵抗的病程。而运用抗体中和等方法降低血液中的Gpnmb可以有效抑制脂肪组织合成脂质的能力,提高机体能量消耗,减轻肥胖并改善胰岛素抵抗。研究揭示了在代谢性疾病等情况下肝脏和脂肪组织的一种通讯机制,也证明靶向Gpnmb可治疗肥胖和糖尿病等。同期杂志发表题为《GPNMB: expanding the code for liver–fat communication》的News & Views进行评论。
根据世界卫生组织统计,2016年,18岁及以上的成年人中逾19亿人超重,其中超过6.5亿人肥胖1。肥胖是糖尿病、脂肪肝和心脑血管疾病的重要危险因素,可受遗传和环境等多因素影响。发现新的“肥胖因子”对于认识和治疗代谢性疾病有重要意义。
机体内的脂质代谢处于动态平衡调控中,sterol-response element binding protein (SREBP)通路可在脂质缺乏时启动甾醇和脂质合成、吸收的基因表达,是其中一个重要的调控通路。之前,宋保亮等在研究中发现,肝脏中特异抑制SREBP通路后可引起脂肪组织的脂质合成增加,从而推测肝脏可分泌某种“肥胖因子”,促进脂肪组织脂质合成2。在本研究中,研究者分析了SREBP通路抑制的小鼠肝脏差异表达基因,对候选基因逐一用腺病毒在小鼠肝脏中过表达,鉴定出Gpnmb可促进脂肪组织合成脂质的能力。Gpnmb通过结合脂肪细胞膜表面的CD44受体上调脂质合成。在小鼠中过表达Gpnmb,可使脂肪重量显著增加,脂肪细胞变大,脂肪组织脂质合成基因显著上调。
那么,这条促进脂肪组织脂质合成的通路有没有可能参与了肥胖的成因和病程发展呢?作者发现过表达Gpnmb可加重小鼠模型中饮食诱导的肥胖,增加脂肪组织重量,提高脂肪组织脂质合成能力,并观察到脂肪组织的产热能力受到抑制,机体的能量消耗降低,加重胰岛素抵抗。而人群中,人血清Gpnmb的浓度与许多肥胖相关的指标(尤其是BMI)呈正相关,并且关联紧密。
进而,作者制备了Gpnmb中和抗体,发现抗体注射能有效逆转肥胖小鼠的表型:减少脂肪组织重量,降低脂肪组织脂质合成基因的表达,促进脂肪组织产热,并减轻胰岛素抵抗。这些研究结果鉴定出Gpnmb是一个新型“肥胖因子”,阐明其作用机理,并验证靶向Gpnmb可治疗肥胖和糖尿病等。
该研究由上海科技大学生命科学与技术学院戚炜课题组与武汉大学生命科学学院宋保亮课题组合作完成,同时得到了上海交通大学医学院宁光院士团队的支持,宋保亮与戚炜为共同通讯作者。该工作获得国家自然科学基金委、科技部重点研发计划经费支持。戚炜博士的主要研究领域为表观遗传与药物研发,研发了组蛋白甲基化酶PRC2的抑制剂,并发现组蛋白去甲基化酶LSD1可抑制Wnt通路从而调控棕色脂肪组织分化发育。自2018年3月入职上科大生命学院后,戚炜实验室的主要研究方向是肿瘤表观药物的分子药理和代谢的表观遗传调控。
文章链接:https://www.nature.com/articles/s42255-019-0065-4
参考文献:
1. World Health Organization, Obesity and overweight. (https://www.who.int/news-room/fact-sheets/detail/obesity-and-overweight)
2. T. F. Liu, J. J. Tang, P. S. Li, Y. Shen, J. G. Li, H. H. Miao, B. L. Li and B. L. Song, Cell Metab, 2012, 16, 213-225.
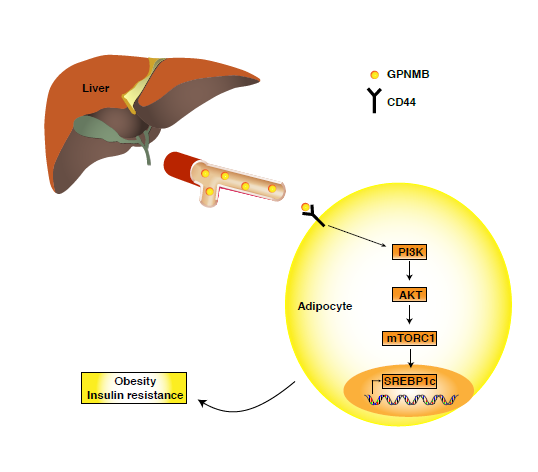
Gpnmb是一个新型“肥胖因子”,可以作为肥胖和糖尿病的药物靶点。肝脏来源的Gpnmb蛋白可激活SREBP,促进脂肪组织的脂质合成,抑制UCP1介导的产热,从而促进肥胖和胰岛素抵抗。


