3月17日,生命学院王彤教授课题组与澳大利亚昆士兰大学Frederic Meunier教授课题组合作在知名学术期刊Journal of Cell Biology(细胞生物学杂志)杂志上在线发表题为“Radial contractility of actomyosin rings facilitates axonal trafficking and structural stability”的研究论文。该研究揭示肌动球蛋白II(None Muscle Myosin II, NM-II)的激活可以控制神经元轴索径向收缩能力,而激活是通过其头部结构域与轴索上呈节段分布的F-肌动蛋白环相关联来实现的。该论文不仅揭示了NM-II马达蛋白的新功能,同时也提示NM-II可能参与神经元轴索的损伤修复。
神经元是人体中最长的细胞。轴索(又称轴突)是神经元伸出的占其99%长度的突起,在神经网络之间起到连接作用,既作为导线传递电信号又作为高速公路介导物质运输。对轴索微小的损伤将会瘫痪整个神经系统,造成如昏迷,神志不清,瘫痪和认知缺陷等神经系统症状。神经元的轴索可以延伸几厘米至一米长,而其直径仅有不到1微米。这种百万级别的轴向和径向的尺度差异使得轴索必须进化出特化的细胞内运输和骨架系统来进行维持。其中,轴索的物质运输主要由Dynein或Kinesin马达蛋白介导的长距离囊泡来实现,而骨架系统的稳定性则是由细胞膜下节段性骨架结构来支撑。然而,这两个重要的分子系统(运输和结构)之间是否存在相互调控和对话仍然未知。
在本研究中作者发现神经元轴索的径向的弹性能够控制大囊泡的运输速度。这种径向的弹性变化由 NM-II控制,对NM-II功能的破坏会影响运输和结构两个系统,导致轴索运输停滞和骨架结构的破坏,并最终导致轴索退行和神经元死亡。该工作首次揭示了NM-II分子在维持轴索的结构和运输两个系统中都扮演着关键的角色。这一新发现,将有助于我们理解神经元这一人体最长的细胞是如何维持其结构的稳定和完整的。对这一机理的深入了解,可以为创伤性脑损伤和诸如帕金森氏症、发性硬化症等神经退行性疾病提供治疗的新手段。
王彤教授是本论文第一作者和共同通讯作者,2019级硕士研究生刘春霞为共同作者。该研究工作得到了澳大利亚科研理事会早期科研生涯发展基金(ARC DECRA),国家自然科学基金面上项目以及上科大科研启动经费的支持。
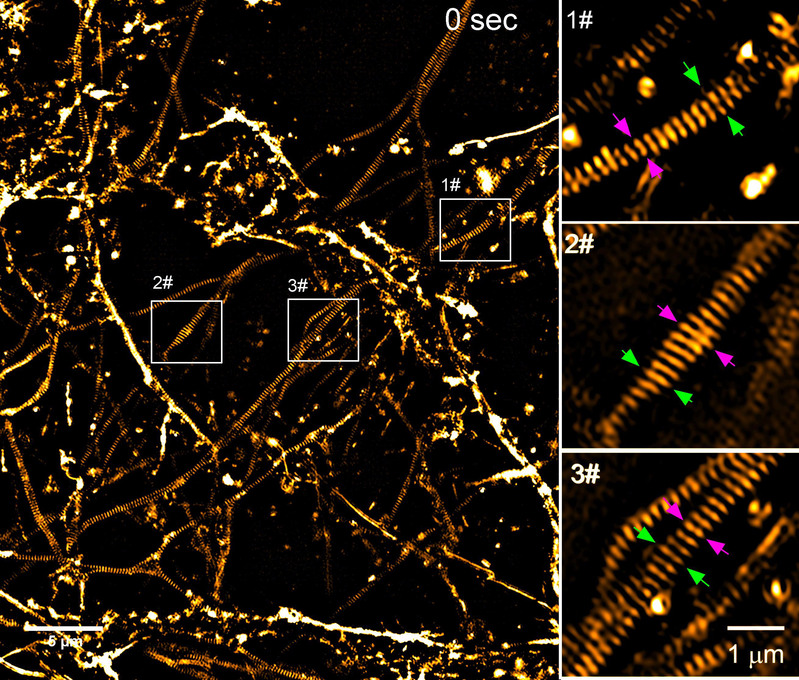
图1:NM-II控制下神经元轴索径向的超分辨率显微图像


