我院黄鹏羽课题组与中国科学院神经科学研究所杨辉课题组合作,利用Cas13d家族蛋白CasRx在小鼠肝脏中实现了Pcsk9基因的高效沉默,从而降低了小鼠血液中的胆固醇水平。很多专家认为,Cas13d在治疗后天性的代谢疾病,抑或新冠病毒SARS-CoV-2和甲流病毒等RNA病毒感染等疾病中具有潜力。然而过去的研究都在体外细胞水平进行。该项工作则首次证实了Cas13d在成体动物体内也具有靶向沉默RNA的活性,从而为Cas13d系统的应用向前推进了一步。3月18日,该研究成果以“Modulation of metabolic functions through Cas13d-mediated gene knockdown in liver”为题在Protein & Cell(《蛋白质和细胞》)杂志发表。
近年来,源自原核生物获得性免疫系统的CRISPR/Cas9技术因其强大且便捷的基因编辑能力而受到广泛关注。CRISPR/Cas9技术通过一个引导RNA(guide RNA)将Cas9蛋白引导至DNA,可以实现对DNA的切割。2016年,张锋实验室又发现了一种新的Cas蛋白Cas13a,可以靶向RNA进行切割(Abudayyeh et al., 2016)。之后人们又陆续发现了靶向RNA的Cas13b, Cas13c和Cas13d(Konermann et al., 2018; Smargon et al., 2017)。由于Cas13家族蛋白靶向RNA的特点,理论上在一些特定疾病的检测和治疗上具有独特的优势,因而成为近年来的研究热点。
Cas13蛋白最直接的应用是靶向沉默RNA。目前Cas13a, Cas13b和Cas13d均被证实可以在哺乳动物细胞系中干扰RNA,从而实现基因沉默(Konermann et al., 2018; Smargon et al., 2017)。其中,2018年由加州大学伯克利分校Patrick Hsu实验室发现的Cas13d家族蛋白CasRx由于体积小,效率高,目前被认为是在未来的应用中最具有优势的Cas13蛋白(Konermann et al., 2018)。与传统的RNAi技术相比,Cas13d介导的基因沉默具有效率高,脱靶率低的优势,从而理论上在疾病治疗过程中具有更高的安全性(Konermann et al., 2018; He et al., 2020)。与Cas9介导的基因敲除技术相比,Cas13d介导的基因沉默不会改变基因组DNA,因此这种基因沉默是可逆的,从而对一些后天性疾病(如因不良生活习惯导致的高血脂等后天代谢性疾病)的治疗更有优势。
Cas13的另一个潜在应用是治疗RNA病毒感染。大量的RNA病毒(如新冠病毒SARS-CoV-2,SARS冠状病毒,MERS冠状病毒,甲流病毒等)在整个生命周期中并不存在DNA。针对于此,最近,美国哈佛大学医学院Pier Paolo Pandolfi教授提出了利用Cas13d系统来治疗新冠病毒感染的可能性(Nguyen et al., 2020)。Pier Paolo Pandolfi实验室对中国、美国、澳大利亚19例新冠病人的病毒基因组分析结果表明,新冠病毒的序列在传播过程中依然在发生变化(Nguyen et al., 2020)。因此靶向新冠病毒的药物和疫苗均存在失效的风险。而Cas13d如果能应用于RNA病毒感染的治疗中,将可以通过改变引导RNA,一方面可以快速响应病毒的新突变,另一方面也可以快速响应新的RNA病毒疫情。
目前关于Cas13的研究都是在体外细胞系中进行的。但更为关键的问题是Cas13是否能在成体动物的体内发挥功能并应用于疾病的治疗。黄鹏羽实验室和杨辉实验室合作将Cas13d系统和靶向Pten基因的guide RNA导入到小鼠肝脏细胞中,成功在肝脏细胞中沉默了Pten基因。他们也观察到在导入Cas13d系统的肝脏细胞中,Pten的沉默增强了下游信号蛋白AKT的磷酸化,并影响了下游相关糖脂代谢相关基因的表达。这说明Cas13d可以应用于模拟体内代谢信号的调控。
相比于其他Cas13蛋白,Cas13d的一个显著优势是体积小,易于包装到AAV病毒当中。在这项研究中,研究者利用AAV将Cas13d系统导入到小鼠肝脏中,降低了胆固醇调控关键基因Pcsk9的表达,并成功地降低了小鼠血液中的胆固醇水平。在这个过程中,研究人员并没有观察到明显的肝损伤,说明Cas13d系统在体内应用时具有一定的安全性。此外,研究者也证实,基于Cas13d的基因沉默是可逆的,这在针对后天性的代谢疾病治疗中具有显著的优势。
中科院神经所研究生贺冰冰、上科大生命学院2015级研究生彭文博、中科院神经所研究生黄佳为共同第一作者。上科大生命学院2018级研究生张航、2016级研究生李志杰等参与了课题研究。上科大生命学院黄鹏羽教授和中科院神经所杨辉研究员为共同通讯作者。该项研究获得了上海科技大学科研启动基金、国家自然科学基金委和科技部的基金支持。
论文链接:https://doi.org/10.1007/s13238-020-00700-2
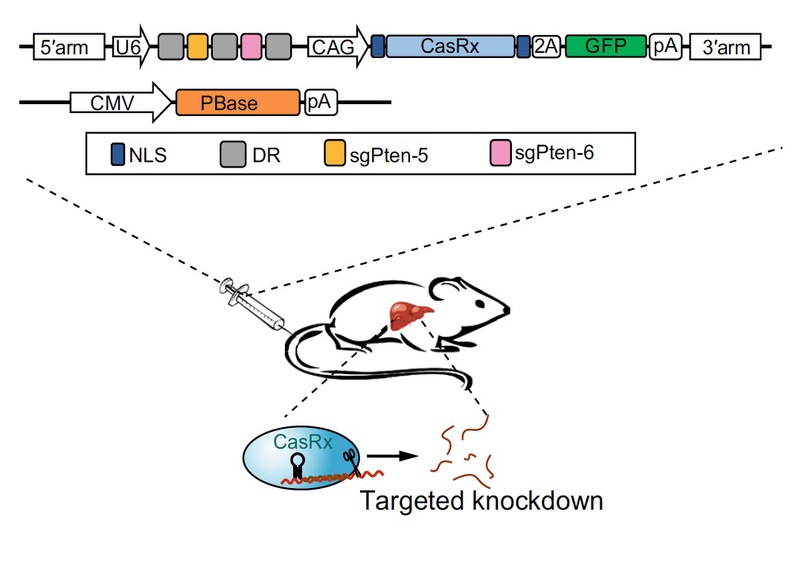
CasRx介导的靶向肝脏RNA降解


