近日,上海科技大学生命科学与技术学院孙博课题组与中国科学院生物与化学交叉研究中心刘聪课题组合作在学术期刊《德国应用化学》(Angewandte Chemie International Edition)上在线发表研究论文,报道了布鲁姆解旋酶(Bloom syndrome helicase,BLM)与单链DNA(single-stranded DNA,ssDNA)互作的新模式。
近年来,在许多生命代谢过程中都观察到了蛋白质相分离(phase separation)现象,而核酸分子被发现广泛参与了调控蛋白质相分离和动态凝聚过程。其中,涉及RNA解旋酶的相分离现象及其相应的体内功能已被深入报道。但与DNA解旋酶相关的相分离研究却十分有限。此外,由于技术上的限制,直接可视化和表征核酸分子与蛋白质在相分离状态下的相互作用仍然具有很高的挑战性。特别是蛋白质如何调控共凝聚体中的核酸,目前还知之甚少。
BLM是RecQ家族中一种重要的DNA解旋酶,广泛参与了维持基因组的完整性和稳定性的代谢过程。BLM的功能缺失、突变可导致一种罕见的常染色体隐性遗传病布鲁姆综合征,具有显着的遗传不稳定性。更重要的是,在多种癌症组织中,如乳腺癌和淋巴瘤等,均发现了高表达的BLM蛋白。BLM的过表达同样被认为与基因组不稳定性密切相关。然而,与BLM过表达相关的基因组不稳定和癌症发病率增加的分子机制仍在很大程度上未知。
研究人员利用荧光光镊技术,在单分子水平上发现了高浓度的BLM蛋白可以在解旋双链DNA(double-stranded DNA,dsDNA)后压缩新生成的ssDNA并形成共凝聚体(图1A)。值得注意的是,在ATP水解的驱动下,由BLM凝聚导致的ssDNA压缩可以抵抗数十皮牛的阻力。此外,BLM还能够通过移除与ssDNA结合的RPA或RAD51蛋白来压缩ssDNA(图1B),这也为BLM作为抗重组酶参与同源重组修复过程中的抗重组功能提供了新的证据。进一步研究表明,单链DNA促进了动态阻滞的BLM凝聚体的形成,导致其可逆性明显降低。
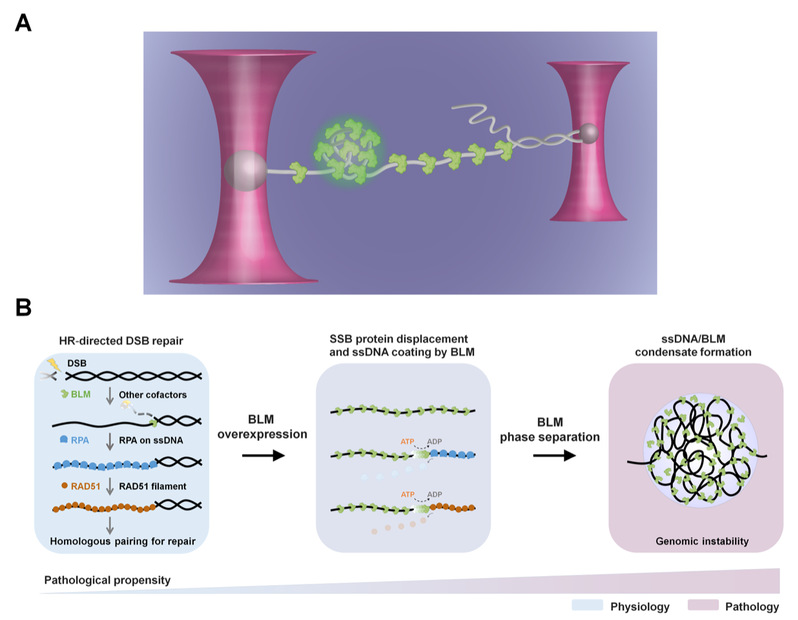
图A| 单分子技术观测BLM解旋dsDNA后压缩ssDNA;
图B| BLM过表达导致的ssDNA压缩和共凝聚干扰HR介导的基因组不稳定模型。
该论文题为“Bloom syndrome helicase compresses single-stranded DNA into phase-separated condensates”(布鲁姆解旋酶通过相分离压缩单链DNA形成共凝聚体),孙博课题组2019级博士生王滕及刘聪课题组2020级博士生胡姣姣为共同第一作者,孙博教授与刘聪研究员为共同通讯作者,上海科技大学为第一完成单位。上科大分子细胞平台的工作人员对该项研究提供了技术帮助。该工作得到了科技部、国自然基金委及上海市科委等基金的支持。
论文链接:
https://onlinelibrary.wiley.com/doi/10.1002/anie.202209463


